Los científicos recorren el cosmos para encontrar los orígenes de los 118 elementos de la tabla periódica
The periodic table turns 150 this year. Here’s how the universe has been filling it with elements for billions of years.
La tabla periódica cumple 150 años este 2019. Así es como el universo la ha estado llenando de elementos durante miles de millones de años.
Desde la invención de la tabla periódica hace 150 años, los científicos han trabajado para completar las filas de elementos y darle sentido a sus propiedades.
Pero los investigadores también han seguido una búsqueda paralela: recorriendo el cosmos para descubrir de dónde provienen los 118 elementos.
Después de siglos de esfuerzo, han determinado que la gran mayoría de los elementos se forjaron en las vidas ardientes y en las extrañas muertes de las estrellas. Ahora impregnan las galaxias, infundiendo diversidad química a la siguiente generación de estrellas y planetas.
De hecho, todos los elementos en la Tierra, excepto unos pocos hechos recientemente por humanos, fueron heredados de la nebulosa que dio a luz a nuestro sistema solar hace 4,500 millones de años. Eso incluye el hierro en nuestros rascacielos, el silicio en nuestras computadoras, el oro en nuestras joyas y el calcio en nuestros huesos.
“Existe una conexión real entre nuestra galaxia, nuestro universo, y nuestra humanidad debido a los elementos”, dijo John Cowan, astrofísico de la Universidad de Oklahoma.
Entonces, ¿cómo llenó la naturaleza la tabla periódica? La historia comienza por el principio.
::
El principio.
A los 15 minutos del Big Bang, los átomos de hidrógeno (número atómico 1) se unieron en la nube de partículas recién nacidas a medida que se expandían y enfriaban. Algunos de ellos se combinaron rápidamente para hacer helio (número atómico 2).
Estos dos elementos aún constituyen el 98% del universo, y son los ingredientes principales de las estrellas. Una astrónoma pionera llamada Cecilia Payne-Gaposchkin descubrió esto cuando publicó la primera estimación precisa de la composición del sol en 1925, anulando la creencia predominante de que era similar a la de la Tierra.
Las primeras estrellas se formaron alrededor de 100 millones de años después del Big Bang, dijo Jennifer Johnson, astrónoma de la Universidad Estatal de Ohio que escribió una reseña de los orígenes elementales en la edición del 1 de febrero de Science para celebrar el sesquicentenario de la tabla periódica.
Estas estrellas eran masivas y, durante millones de años, generaron energía al “quemar” hidrógeno, combinando átomos en helio a través de la fusión nuclear, tal como lo hace el sol en la actualidad.
Sin embargo, eventualmente todas las estrellas se quedan sin combustible de hidrógeno. Luego comienzan a hacer elementos cada vez más pesados a un ritmo cada vez más frenético, poblando las siguientes tres filas de la tabla periódica en el proceso.
Por un tiempo, queman helio en carbono (número atómico 6) y oxígeno (número atómico 8). En los siglos finales de la vida de una estrella masiva, convierte el carbono en elementos como el sodio (número atómico 11) y el magnesio (número atómico 12).
En las últimas semanas, los átomos de oxígeno se fusionan en silicio (número atómico 14), fósforo (número atómico 15) y azufre (número atómico 16). Y en los últimos días de la vida muy larga de una estrella, produce metales como el hierro (número atómico 26).
Hay algo maravillosamente prosaico en eso, dijo Johnson. “Eso es una escala de tiempo humana”.
Luego viene lo que los astrónomos llaman siniestramente “catástrofe de hierro”. La fusión no puede combinar elementos más pesados que el hierro, por lo que la estrella se queda sin jugo.
“Va en caída libre”, describió Johnson.
En menos de un segundo, la estrella se derrumba sobre sí misma y luego explota como una supernova, arrojando sus elementos recién acuñados al universo.
Las supernovas también pueden desatar rayos cósmicos que separan átomos más grandes para crear litio (número atómico 3), berilio (número atómico 4) y boro (número atómico 5). Este proceso es la fuente principal de estos elementos en el universo.
::
El hecho de que los elementos hasta el hierro fueron cocinados en estrellas ha sido más o menos establecido durante décadas, gracias al trabajo del astrónomo británico Fred Hoyle. Los orígenes del resto de los elementos han sido más difíciles de precisar.
El comienzo de una respuesta llegó en un artículo histórico de 1957 escrito por la astrónoma de Caltech, Margaret Burbidge, y su esposo, George, junto con Hoyle y otro científico prominente, William Fowler. (El documento, que comienza con las reflexiones de Shakespeare sobre las estrellas, se ha vuelto tan famoso que los científicos simplemente lo llaman B2FH, por las iniciales de sus autores).
Los elementos pesados se forman cuando un átomo de semilla como el carbono o el hierro es bombardeado con neutrones y los captura en su núcleo.
“Se los traga a todos”, dijo Anna Frebel, astrónoma del MIT. “Entonces la pregunta es, ¿le gusta o no? Y por lo general, no lo hace”. Entonces, el átomo sufre un decaimiento radioactivo y, en última instancia, emerge como un elemento más pesado y más estable.
B2FH estableció la física de cómo este proceso podría suceder rápida o lentamente.
Un candidato obvio para el proceso rápido fue el caos de una supernova. Pero en los últimos años, los científicos han comenzado a cuestionar esa idea. “Probablemente no haya suficiente empuje, incluso en una explosión de supernova masiva para crear todos estos elementos”, dijo Frebel.
Parte de la evidencia proviene de la investigación de Frebel sobre una pequeña galaxia que contenía montones de oro y otros elementos pesados. Si todos ellos hubieran sido el resultado de supernovas, hubieran requerido tantos que “vas a destruir la galaxia”, sostuvo.
En cambio, los científicos han comenzado a favorecer un fenómeno diferente: las fusiones entre las estrellas de neutrones.
Las estrellas de neutrones son esferas ultra densas que quedan tras la muerte de estrellas masivas. Pueden tener diámetros tan pequeños como 12 millas y masas de hasta 2,5 veces la del sol. De vez en cuando, dos de ellos se encierran en un tango mortal, en espiral hacia el otro hasta que chocan.
Estas fusiones liberan una lluvia de neutrones lo suficientemente intensa como para crear los elementos más pesados del universo, como el uranio (número atómico 92) y el plutonio (número atómico 94).
Esta idea se reforzó en 2017, cuando el Observatorio de Ondas Gravitacionales del Interferómetro Láser detectó una colisión de estrellas de neutrones por primera vez. Los investigadores estudiaron la luz de la explosión y encontraron las huellas reveladoras de elementos pesados, incluido el oro.
Los científicos todavía tienen que resolver los roles relativos de las fusiones de superovas y de estrellas de neutrones. Pero Frebel dijo que los científicos están cada vez más cerca de entender la fuente de cada elemento.
“La última gran brecha se ha cerrado”, dijo. “Eso es simplemente bueno”.
::
Las primeras fusiones de estrellas de neutrones ocurrieron después de que la primera generación de estrellas muriera, y salpicaron el cosmos con todo tipo de nuevos átomos.
Eso incluye a algunos que son tan inestables que no existen en nuestro sistema solar en la actualidad, excepto por unos pocos milisegundos en el laboratorio de un investigador.
“Has hecho mucho ruido todo el camino a través de la tabla periódica”, dijo Johnson. “Así que dentro de unos 200 millones de años después del Big Bang, has hecho algunos de cada elemento”.
Pero la composición del universo siguió cambiando. Durante los siguientes mil millones de años, los nuevos procesos cósmicos comenzaron a aumentar la abundancia de ciertos elementos a medida que las estrellas más pequeñas comenzaron a formarse.
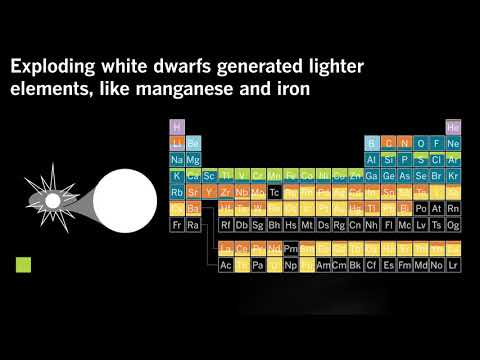
Estas estrellas no son lo suficientemente grandes para producir nada más pesado que el carbono y el oxígeno, o para explotar como supernovas masivas. En cambio, cuando cesa la fusión en sus núcleos, se convierten en enanas blancas.
Las enanas blancas pueden chocar, provocando un proceso de fusión fuera de control que convierte casi todo en la estrella en hierro. “Puedes crear básicamente una bomba de hierro”, dijo Frebel.
Antes de eso, durante sus muertes prolongadas, algunas estrellas de poca masa también pueden incubar elementos pesados. Los neutrones que quedaron de sus días de quema de helio se adueñan de los núcleos de otros elementos a razón de uno en pocas semanas o meses, formando gradualmente átomos más pesados que avanzan lentamente por la tabla periódica.
Se requieren más de 100 neutrones capturados para convertir un átomo de hierro en un elemento de tierras raras como el lantano (número atómico 57) o lutecio (número atómico 71). Sin embargo, hay muchas de estas estrellas, y permanecen durante mucho tiempo, por lo que producen aproximadamente la mitad de los elementos más pesados que el hierro.
Un astrónomo llamado Paul Merrill encontró evidencia de este proceso en 1951. Trabajando en el Observatorio Mount Wilson sobre Los Ángeles, identificó el tecnetio del elemento radioactivo (número atómico 43) en una estrella antigua y enfermiza.
Los científicos sabían que el tecnecio era inestable y decayó rápidamente. Eso significaba que no podría haber sido heredado por una estrella que ya tenía miles de millones de años, pensó Merrill. La única forma en que el elemento podría haber llegado allí era si la estrella lo hubiera logrado.
::
Hoy, 13.8 mil millones de años después del Big Bang, las estrellas han convertido aproximadamente el 2% del hidrógeno y el helio del universo en otros elementos.
Ahora existen en cantidades variables, dependiendo de la frecuencia y la productividad de los procesos que los crean. El platino (número atómico 78), por ejemplo, es un millón de veces más raro que el hierro porque las fusiones de estrellas de neutrones no ocurren muy a menudo. (Esa es una razón por la cual los metales preciosos son preciosos, dijo Cowan.)
La presencia de elementos como el carbono y el oxígeno ayudó a enfriar los rincones de la galaxia para que pudieran formarse estrellas más pequeñas como el sol. Y la aparición de metales permitió que los sistemas solares emergieran de los discos de gas y polvo que giraban alrededor de estas nuevas estrellas.
“Ahora hay suficiente basura en el disco para que puedas formar planetas”, dijo Johnson. “Cuanto más hierro se compara con el hidrógeno, más probabilidades tenemos de encontrar un Júpiter”.
La proporción creciente de hierro a elementos como el oxígeno también incrementó las posibilidades de formar planetas rocosos con núcleos grandes, como la Tierra. (Los núcleos grandes pueden cumplir muchas funciones, incluida la generación de un campo magnético que protege la vida).
A medida que el universo envejece, los elementos dentro de él se volverán más pesados. Y en aproximadamente 10 billones de años, cuando la formación estelar haya fracasado, su composición dejará de cambiar.
Hay un debate sobre cuánto hidrógeno quedará en ese punto. Johnson cree que una buena cantidad permanecerá en el medio intergaláctico, mientras que Frebel sospecha que la mayor parte se habrá transformado.
Pero seguirá existiendo en otro sentido, dijo, ya que todos los elementos son solo reordenamientos de los átomos de hidrógeno que se formaron en los primeros minutos después del Big Bang. Han estado dando vueltas alrededor del cosmos desde entonces, en un elemento u otro. Algunos terminaron aquí en la Tierra, donde hacen todo. Incluyéndonos a nosotros.
Al querido astrónomo Carl Sagan le gustaba decir que “estamos hechos de estrellas”.
Eso no es todo, Fredel dijo: “También somos cosas del Big Bang”.
Para leer esta nota en inglés, haga clic aquí.
Suscríbase al Kiosco Digital
Encuentre noticias sobre su comunidad, entretenimiento, eventos locales y todo lo que desea saber del mundo del deporte y de sus equipos preferidos.
Ocasionalmente, puede recibir contenido promocional del Los Angeles Times en Español.




